Soal Thermodinamika
Hitung perubahan entropi dari 30 gram alumunium yang dipanaskan dari
500 sampai 700 OC. Titik leleh 660 OC, kalor pelelehan 393 J g-1 dan
kapasitas kalor zat padat dan zat cair masing-masing adalah : (31,8 +
3,15 .10-3 T) JK-1 mol-1 dan (34,3 + 1,12 .10-3 T) JK-1 mol-1.
Jawaban :
Ada tiga tahapan disini.
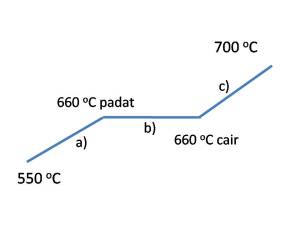
Pertama : alumunium memanas dari suhu 500 ke 660
Kedua : alumunium mencair dari 660 dalam wujud padat menjadi 660 dalam wujud cair. Ada panas latent yang berperan
Ketiga : alumunium dalam wujud cair memanas dari suhu 660 menjadi 700 oC
Gambar dari prosesnya adalah :
m = 30 g
panas Latent pelelehan (L) = 393 j/gram
path (a)
Cp = 31.8 + 3.15 x10-3 T
ΔS = mCp(dT/T) masukkan Cp dan diintegralkan diperoleh
ΔS = mx(31.8 ln(T/T0) + (3.15/2)x10-3(T-T0)
ΔSa = 272,4206767 j/K
path (b)
ΔH = mxL
ΔH = 30 x 393 = 11790 j
ΔSb = ΔH /T = 11790 j/660 K
ΔSb = 17,86363636 j/K
path (c)
Cp = 34.3 + 1.12 x10-3 T
ΔS = mCpdT/T masukkan Cp dan diintegralkan diperoleh
ΔS = mx(34.3 ln(T/T0) + (1.12/2)x10-3(T-T0)
ΔSc = 61,21887452 j/K
S total = Sa + Sb + Sc
S total = 272,4206767 + 17,86363636 + 61,21887452 j/K
S total = 351,5031876 j/K
Jawaban :
Ada tiga tahapan disini.
Pertama : alumunium memanas dari suhu 500 ke 660
Kedua : alumunium mencair dari 660 dalam wujud padat menjadi 660 dalam wujud cair. Ada panas latent yang berperan
Ketiga : alumunium dalam wujud cair memanas dari suhu 660 menjadi 700 oC
Gambar dari prosesnya adalah :

m = 30 g
panas Latent pelelehan (L) = 393 j/gram
path (a)
Cp = 31.8 + 3.15 x10-3 T
ΔS = mCp(dT/T) masukkan Cp dan diintegralkan diperoleh
ΔS = mx(31.8 ln(T/T0) + (3.15/2)x10-3(T-T0)
ΔSa = 272,4206767 j/K
path (b)
ΔH = mxL
ΔH = 30 x 393 = 11790 j
ΔSb = ΔH /T = 11790 j/660 K
ΔSb = 17,86363636 j/K
path (c)
Cp = 34.3 + 1.12 x10-3 T
ΔS = mCpdT/T masukkan Cp dan diintegralkan diperoleh
ΔS = mx(34.3 ln(T/T0) + (1.12/2)x10-3(T-T0)
ΔSc = 61,21887452 j/K
S total = Sa + Sb + Sc
S total = 272,4206767 + 17,86363636 + 61,21887452 j/K
S total = 351,5031876 j/K
Ada yang salah enggak?
ReplyDelete